Na rynku leków biologicznych i biopodobnych polskie firmy specjalizują się przede wszystkim w produkcji insulin i szczepionek. Istnieje również kilka przedsiębiorstw pracujących nad ciekawymi, niszowymi projektami. Wydaje się, że w kwestii leków biopodobnych firmy rodzime mogłyby skorzystać na wygasaniu światowych patentów na te leki, podobnie jak to uczyniły w przypadku leków klasycznych. Barierą mogą być jednak bardzo wysokie koszty produkcji leków biologicznych, wynika z najnowszego raportu PMR „Rynek leków biologicznych i biopodobnych w Polsce 2013. Prognozy rozwoju na lata 2013-2015".
Polskie firmy mało konkurencyjne na rynku leków biologicznych
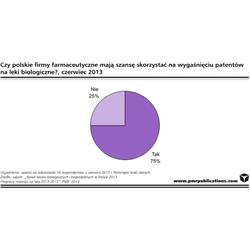
W badaniu przeprowadzonym specjalnie na potrzeby raportu PMR zapytał firmy o to, czy w ich opinii polskie przedsiębiorstwa mają szanse skorzystać na trendzie wygasania patentów na leki biologiczne. Okazuje się, że trzy czwarte respondentów uważa, że tak, pod warunkiem że będą miały odpowiednie know-how, linie produkcyjne, laboratoria, co nie jest, jak zaznaczają respondenci, prostą sprawą. Sytuację ułatwi natomiast obecny kierunek polityki refundacyjnej, nastawionej na tańsze odpowiedniki oryginalnych leków. W naszej opinii, będzie to jednakowoż szansa głownie dla większych koncernów, które mają środki na inwestycje, głównie zagranicznych.
Respondenci wyrażają również obawę przed konkurencją z Chin, gdzie firmy farmaceutyczne przygotowują już się na moment wygaśnięcia patentów, jak również biurokracją w urzędach polskich (chodzi tu głównie o prowadzenie badań klinicznych).
Pojawienie się biopodobnych przeciwciał monoklonalnych w Polsce kwestią czasu
W połowie 2013 r. EMA zarekomendowała do dopuszczenia do obrotu pierwsze biopodobne przeciwciała monoklonalne Remsima (Celltrion Healthcare Hungary Kft) oraz Inflectrę (Hospira UK Limited) zawierające substancję infliksymab. Lekiem oryginalnym jest Remicade zarejestrowany w UE w 1999 r. Leki zarekomendowano w tych samych wskazaniach – w szeregu chorób o podłożu autoimmunologicznym, w tym reumatoidalnym zapaleniu stawów, chorobie Crohna, zapaleniu okrężnicy, łuszczycy, łuszczycowym zapaleniu stawów i ZSSK.
Regulacje dla rejestracji przeciwciał monoklonalnych obowiązują od grudnia 2012 r. Wydaje się więc, że i pojawienie się biopodobnych przeciwciał monoklonalnych w Polsce pozostaje kwestią czasu.
Wśród kandydatów na biopodobne przeciwciała monoklonalne wymienia się również, m.in.:
- transtuzumab (Herceptin)
- bevasizumab (Avastin)
- rituximab (MabThera)
- cetuximab (Erbitux)
- adalimumab (Humira)
- palivizumab (Synagis).
Niniejsza informacja prasowa została przygotowana na podstawie danych zawartych w najnowszym raporcie firmy PMR pt. „Rynek leków biologicznych i biopodobnych w Polsce 2013. Prognozy rozwoju na lata 2013-2015".
- Autor:
- Monika Stefańczyk Główny analityk rynku farmaceutycznego
- Źródło:
- PMR
Komentarze (0)
Czytaj także
-

AUTOMATYZACJA POMIARU PH I STĘŻENIA JONÓW NIEORGANICZNYCH W PROCESIE PRZY...
Każdego dnia na całym świecie wykonywanych jest tysiące pomiarów pH oraz oznaczeń kationów i anionów w przeróżnych matrycach. Często cała...
-

Produkcja kontraktowa suplementów diety – model współpracy, który zmienia rynek
Jeszcze kilka lat temu wystarczyło mieć pomysł na produkt i sprawny marketing. Dziś to już nie działa. Rynek suplementów diety dojrzał, a wraz z...
-

-

-