Fluorek miedzi (I), uznawany od wielu lat za niestabilny związek, który jest „brakującym półprzewodnikiem" pomiędzy tlenkiem cynku i azotkiem galu można otrzymać i co więcej będzie on miał inną budowę niż ustalono w prawie 80 lat temu.
Aron Walsh z University of Bath w Wielkiej Brytanii dokonał obliczeń teoretycznych budowy fluorku miedzi CuF. W literaturze związek ten pojawia się tylko w formie krótkiej informacji o jego syntezie w 1933 r. i strukturze sfaleritu. Obliczenia komputerowe pokazały, że taka struktura nie jest stabilna w związku z tym nie udałoby się otrzymać CuF w takiej formie. Dlatego rozpoczęto poszukiwania innych struktur CuF.
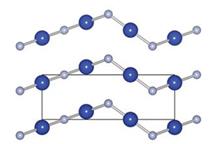
Jedną z najstabilniejszych struktur okazała się orientacja liniowych łańcuchów CuF w chiralnym ułożeniu jak dla kryształu cynobru (układ trygonalny). Fluorek miedzi (I) okazuje się mieć optyczne właściwości i przewodność oraz potencjał jonizacji, dzięki którym po dodaniu ZnO lub CuO2 można byłoby stworzyć pasmo typu II, służące do zamiany energii świetlnej w energię elektryczną. Znając stabilną postać CuF można pokusić się o zaprojektowanie drogi jego syntezy.
W opinii Mike Nolana z University College Cork w Irlandii opisanie struktury fluorku miedzi (I) jest dobrym przykładem siły nowoczesnej chemii obliczeniowej, która może służyć do projektowania a następnie syntezy nowych materiałów.
(pj)
Kategoria wiadomości:
Z życia branży
- Źródło:
- rsc.org

Komentarze (0)
Czytaj także
-

Robotyczna prostatektomia da Vinci – nowoczesne podejście w leczeniu raka...
Prostatektomia radykalna z użyciem systemu robotycznego da Vinci to jedna z najnowocześniejszych metod leczenia raka gruczołu krokowego. Łączy...
-

Rozwój leków: kluczowa rola chromatografii jonowej w opracowywaniu nowych...
W procesie opracowywania nowych leków każda technologia analityczna odgrywa istotną rolę w zapewnieniu jakości i bezpieczeństwa produktu....
-

-

-





